张青松1, 查刘生1,2, 马敬红1, 梁伯润1
(1.东华大学纤维材料改性国家重点实验室,上海200051;2.东华大学分析测试中心)
温敏性微凝胶是粒径在10~1000nm,能响应环境温度变化发生相转变的聚合物胶体粒子。温敏性微凝胶在水介质中发生相转变的同时,往往伴随着体积、亲水性、表面电荷密度和胶体稳定性等许多物理性质的变化[1],因而在药物控制释放,生物物质分离,酶固定化及其活性可控等许多方面有诱人的应用前景[2~3]。温敏性微凝胶分子结构中通常含有一定比例的疏水基团和亲水基团,温度的变化会破坏亲水基团与水之间的氢键作用,从而引起分子链的亲水性发生改变,导致微凝胶在水介质中产生体积相转变[4]。温敏性微凝胶发生体积相转变时的温度称为体积相转变温度(VPTT)。目前的温敏性微凝胶研究主要集中在以N-异丙基丙烯酰胺(NIPAM)为主要单体的均聚物或共聚物微凝胶上,它们的VPTT在33°C左右[5~6],处于生物物质可以保持活性的温度范围内,因而受到国内外许多高分子科学工作者的高度关注。VPTT是温敏性微凝胶最重要的性能参数,它反映了微凝胶分子链的亲水性,并决定了温敏性微凝胶的使用范围。通常采用NIPAM与其他单体共聚的方法来调节聚(N-异丙基丙烯酰胺)/(PNI-PAM)微凝胶的VPTT:NIPAM与亲水单体共聚,微凝胶的VPTT会上升[7];NIPAM与疏水单体共聚,微凝胶的VPTT会下降[8]。由于NIPAM是水溶性单体,因此通过无皂乳液聚合方法很容易与其他亲水单体共聚合成温敏性微凝胶,但与疏水单体共聚往往比较困难。唐小真等[9]人采用疏水性较弱的甲基丙烯酸乙酯与NIPAM共聚合成温敏性微凝胶,随着疏水性单体用量的增加,微凝胶的VPTT下降。而Chowdhry等[10]人发现用疏水性很强的乙烯基月桂酸酯单体与NIPAM共聚合成的核壳结构的温敏性微凝胶的VPTT与疏水单体的用量关系不大。
本文采用一种疏水性较强的丙烯酸叔丁酯(tBA)单体与NIPAM单体共聚合成了P(NIPAM-co-tBA)微凝胶,该微凝胶经水解后可使酸根离子分布于微凝胶内部,从而达到pH和温度双重敏感的目的。通过傅立叶变换红外光谱、扫描电镜和动态光散射等手段表征了所得微凝胶的化学和形态结构以及温度敏感性,初步研究结果表明:该微凝胶具有良好的单分散性和温敏性,且体积相转变温度和溶胀比均随tBA含量的增加呈明显的下降趋势。
1 实验部分
1.1 原料和试剂
N-异丙基丙烯酰胺(NIPAM):东京化成,纯度95%,用甲苯/环己烷(体积比60/40)混合溶剂重结晶纯化,25°C真空干燥后备用;丙烯酸叔丁酯(tBA):东京化成,减压蒸馏处理;N,N′-亚甲基双丙烯酰胺(MBA):Fluka公司,甲醇中重结晶;过硫酸铵(APS):中国医药集团上海化学试剂有限公司,分析纯,用乙醇重结晶。
1.2 P(NIPAM-co-tBA)微凝胶的制备和纯化
将一定比例的NIPAM、MBA溶于150mL去离子水中,用微量移液器注射不同含量的tBA,加入装有冷凝管、恒压滴液漏斗、温度计和通氮气口的四口烧瓶中,搅拌下通氮气除氧30min。加热升温至70°C,滴加一定量的APS水溶液,反应即开始。几分钟后体系由透明变成淡蓝色,然后慢慢变成乳白色。恒温70°C反应6h,整个反应过程中持续通氮气。反应物投料比见表1。

将得到的乳液用高速离心机离心分离,弃去上层清液后,用超声波振荡仪将微凝胶重新分散在去离子水中,如此重复3次,即可除去体系中存在的少量水溶性聚合物、残余单体和交联剂。
1.3 P(NIPAM-co-tBA)微凝胶的结构表征和性能测试
1.3.1 傅立叶变换红外光谱(FT-IR)
将纯化好的微凝胶乳液冷冻干燥后,研磨成粉末,与KBr混合后压成样片,用傅立叶变换红外光谱仪(Nicolet,NEXUS-670)测定其红外光谱。
1.3.2 扫描电子显微镜(SEM)
将纯化好的微凝胶乳液滴在盖玻片上,干燥后对样品表面进行喷金处理,用JSM-5600LV型扫描电镜(JEOL,Japan)观察微凝胶在真空干燥状态下的形貌和粒径的分布情况。1.3.3 动态激光光散射(DLLS) 微凝胶在不同温度下的水动力学直径(DH)采用动态激光光散射仪(Malvern,Mastersizer2000)测试,激光波长为532nm,散射角为90°。微凝胶乳液用去离子水稀释后,在每一温度下至少平衡10min,以保证微凝胶在水介质中达到溶胀-消溶胀平衡。取3次测量结果的平均值为微凝胶的DH。
1.3.4 溶胀比(α) 溶胀比α即发生体积相转变前后的体积之比,是温敏性微凝胶的重要性能参数之一[11]。本文通过测定微凝胶在5°C和50°C下的水动力学直径DH,根据如下公式计算P(NIPAM-co-tBA)微凝胶的溶胀比:

2 结果与讨论
2.1 P(NIPAM-co-tBA)微凝胶形成的机理及其结构确证
本文采用无皂乳液聚合方法使亲水的NIPAM单体和MBA交联剂与疏水的tBA单体共聚合成温敏性微凝胶。少量的tBA通过注射加入到NIPAM和MBA的水溶液中,通过搅拌形成分散液。由于NIPAM分子结构中具有明显的亲水基团(酰胺基团)和疏水基团(异丙基),这对加入的tBA可能有一定的增溶作用,形成大量的分子聚集数目不多的微胶束。一般来说,丙烯酰胺类单体的反应活性比丙烯酸酯类高,因此滴加引发剂水溶液后,将首先引发溶解在水中的单体NIPAM和交联剂MBA聚合,形成低聚物P(NIPAM-co-MBA)自由基链。由于反应温度(70°C)在PNIPAM的最低临界溶解温度(LCST≈32°C)之上,形成的P(NIPAM-co-MBA)低聚物自由基链增长到一定长度后,将发生线团-小球转变,形成类似其他无皂乳液聚合体系成核期生成的初级粒子。该初级粒子内部具有明显的疏水性,结果使得反应体系中被NIPAM增溶的tBA将逐渐转移到初级粒子内部,和其中吸收的NIPAM与MBA一起进行链增长反应,使初级粒子逐渐长大并最终形成微凝胶胶体粒子。由引发剂(APS)分解碎片形成的离子基团(―SO2-4)位于微凝胶粒子表面,通过静电排斥作用使其处于胶体稳定状态。
图1是合成的微凝胶的傅立叶变换红外光谱图。所有谱线均在1650、1547和1273cm-1处存在酰胺 带、 带、 带的特征峰,它们分别是CO伸缩振动峰,N―H面内弯曲振动频率与部分C―N键的伸缩振动频率耦合产生的吸收峰和C―N伸缩振动峰。同样,在1388cm-1和1368cm-1处,均存在因异丙基上双甲基的对称弯曲振动耦合分裂而形成的强度几乎相等的双峰。但样品的谱线比较表明,使用单体tBA与NIPAM、MBA共聚合成的微凝胶在1726cm-1处存在酯羰基(CO)伸缩振动吸收峰,而且峰的强度随tBA用量的增加而增加。红外光谱分析结果表明,单体tBA与NIPAM、MBA共聚合成的微凝胶具有图2所示的化学结构。

2.2 P(NIPAM-co-tBA)微凝胶的形状和单分散性
图3是PNIPAM均聚物微凝胶和P(NIPAM-co-tBA)共聚物微凝胶纯化后的SEM照片。从图上可以看出,微凝胶粒子均呈球形形状,单分散性较好,说明粒子成核按上述机理进行,成核期很短,无二次成核过程。随着共聚单体tBA用量的增加,微凝胶粒径呈下降趋势。
2.3 P(NIPAM-co-tBA)微凝胶的相转变行为
图4是P(NIPAM-co-tBA)微凝胶的DH随温度变化的曲线。从图中可以看出,和PNIPAM微凝胶一样,P(NIPAM-co-tBA)微凝胶的DH在一定温度范围内随着温度增加而急剧下降,即发生了体积相转变,表明P(NIPAM-co-tBA)微凝胶具有温敏性。一般将温敏性微凝胶的DH~t曲线上的拐点对应的温度定义为它的体积相转变温度(VPTT),由此测出温敏性微凝胶MG0、MG16、MG24、MG32、MG48的VPTT分别约为33、28、25、22、18°C。随着共聚单体tBA用量的增加,P(NI-PAM-co-tBA)微凝胶的VPTT逐渐下降。

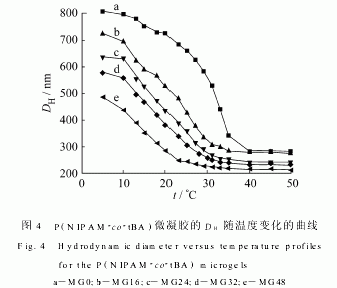
这一现象首先说明tBA与NIPAM共聚形成的是无规共聚结构,而不是嵌段共聚结构,其原因在于嵌段结构不会改变产物的VPTT;tBA单元在微凝胶内部分布应该是均匀的,而不是富集在内核形成核壳结构。另外P(NIPAM-co-tBA)分子链中引入的tBA单元具有较强的疏水性,它破坏了PNIPAM分子链原有的亲水-疏水平衡,使P(NIPAMco-tBA)微凝胶与水之间的氢键作用减弱,破坏该氢键作用所需要的能量降低,从而使P(NIPAM-cotBA)微凝胶可在较低的温度下发生相转变。tBA单元含量越高,P(NIPAM-co-tBA)分子链的疏水性越强,相应微凝胶的VPTT越低。与文献[9]的研究结果进行比较可以看到,由于单体tBA的疏水性比甲基丙烯酸乙酯(EMA)强,tBA共聚组分使温敏性微凝胶VPTT降低的效果比EMA大。从图4中还可以发现,随着tBA单元含量的增加,P(NIPAM-co-tBA)微凝胶的相转变温度范围越来越宽,微凝胶粒径下降的幅度也越来越小,表明微凝胶的温敏性逐渐降低。这是由于tBA单元本身不具有温敏性,PNIPAM分子链中过多引入非温敏性单元,必然导致微凝胶的温敏性逐渐减弱。2.4 P(NIPAM-co-tBA)微凝胶的溶胀比
用DLLS测得的P(NIPAM-co-tBA)微凝胶在5°C和50°C下的DH及由此计算出的溶胀比见表。从表中可以看出,tBA含量对5°C时P(NIPAM-co-tBA)微凝胶的DH影响较大,而对50°C时的H影响较小。当P(NIPAM-co-tBA)微凝胶处于VPTT温度以下,随着凝胶网络分子链中亲水的IPAM单元被疏水的tBA单元取代,微凝胶内部疏水性增加,吸水能力减弱。另外分子链疏水性增加,致凝胶收缩的分子链之间的疏水作用加强。因此,随着P(NIPAM-co-tBA)微凝胶中tBA组分含量增,它在VPTT温度以下的DH逐渐减小。在VPTT温度以上,由于P(NIPAM-co-tBA)分子链中的IPAM单元本身有疏水性,因此引入疏水的tBA单元对分子链的亲疏水性影响不大。

保持主单体NIPAM和交联剂MBA的用量不变,改变共聚单体tBA的用量(见表1),P(NIPAM-co-tBA)微凝胶在收缩状态下的粒径变化不大,说明无皂乳液聚合反应初期形成的初级粒子数目相近,共聚单体tBA对微凝胶的成核过程影响很小。以上分析说明:表2中P(NIPAM-co-tBA)微凝胶的溶胀比随着tBA组分含量增加出现明显下降趋势的原因。
3 结 论
(1)通过改进的无皂乳液聚合方法制备了P(NIPAM-co-tBA)微凝胶,该微凝胶具有良好的单分散性和温度敏感性。
(2)随着tBA用量的增加,P(NIPAM-co-tBA)微凝胶的体积相转变温度和溶胀比下降,温度敏感范围变宽,但过多的tBA用量会导致微凝胶的温度敏感性消失。
|